本研究由薛立祥教授(北京大学第三医院肿瘤中心、北京大学第三医院基础医学研究中心)牵头。在卵巢癌中,多不饱和脂肪酸(PUFA)代谢中多种代谢酶的异常表达参与肿瘤的发生发展和免疫调节。由于症状隐蔽、早期不易发现,大多数患者入院时已是晚期。对标准铂类化疗的耐药性进一步导致生存率低。“有必要建立有效的预后模型并寻找关键的肿瘤标志物,以进一步指导卵巢癌的临床实践并提高患者的生存率,”薛说。
该团队基于PUFA相关基因建立了卵巢癌的10个基因特征预后模型。该模型具有很强的鲁棒性,能够在不同平台(TCGA、ICGC、GSE17260)的数据集中发挥稳定的预测作用。
研究人员进一步利用临床样本验证了这些PUFA相关基因的表达与患者预后或免疫浸润之间的相关性。他们发现LTA4H的高表达表明卵巢癌患者预后不良,并且与CD8 +细胞浸润减少和CD11b +细胞浸润增加相关。LTA4H 参与花生四烯酸 (AA) 衍生物白三烯 B4 (LTB4) 的生产。“这些结果表明 LTA4H 在卵巢癌中发挥负面作用,并参与免疫调节,”薛说。
研究团队进一步证实LTA4H在多种卵巢癌细胞中高表达。体外实验表明,通过基因敲低或抑制剂靶向LTA4H可以显着抑制卵巢癌细胞和类器官的增殖。此外,他们发现抑制LTA4H可以显着增加卵巢癌细胞中CCL5的表达和分泌,这可能与LTA4H对DNA甲基转移酶DNMT1的正向调节有关。
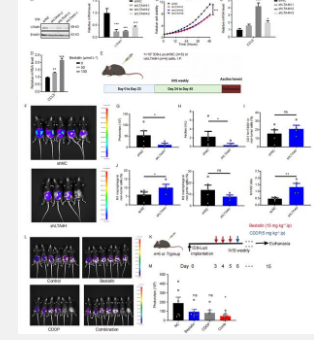
最后,他们发现靶向 LTA4H 可显着抑制体内肿瘤生长,并增加对顺铂治疗的敏感性。靶向 LTA4H 通过上调肿瘤微环境中 M1 巨噬细胞的比例来改善免疫微环境。“这些令人兴奋的新结果揭示了 AA /LTA4H/CCL5 如何确定对顺铂的敏感性和卵巢癌免疫表型的层次结构,”Xue 说。
AA 代谢作为 PUFA 代谢的一个特征途径,在卵巢癌中被发现受到干扰,但其作用尚未明确阐明。该研究明确了LTA4H在卵巢癌中的免疫调节功能,为靶向LTA4H作为卵巢癌新的治疗策略提供了实验证据。